SARS-CoV-2的T细胞表位定位揭示IFN-γ协同产生和T细胞克隆扩增促进COVID-19的恢复
### 背景
在严重急性呼吸综合征冠状病毒2 (SARS-CoV-2)感染期间,T细胞反应可能是保护性的,也可能是有害的。然而,人们对其潜在机制知之甚少。
### 方法
在本研究中,我们在9名实验室确诊的2019冠状病毒病(COVID-19)患者(5名中度病例和4名重度病例)和9名健康捐献者(HD)的外周血单核细胞 (PBMC) 中筛选了144个15肽,这些肽涵盖了SARS-CoV-2刺突蛋白、核衣壳 (NP)、M、ORF8、ORF10和ORF3a 蛋白,以及39个已报道的SARS-CoV-1肽,这些患者均在COVID-19大流行之前收集。使用ELISA 通过IFN-γ和IL-17A的产生来监测T细胞应答,并对阳性样本进行T细胞受体 (TCR)β 链测序。通过流式细胞术验证了对单个SARS-CoV-2 肽的阳性T细胞应答。
### 结果
**1、中度疾病患者的T细胞对SARS-CoV-2抗原有较强的应答**
(A)总体研究设计示意图。(B)培养上清中的IFN-γ采用ELISA法检测HD和COVID-19中重度患者外周血单核细胞,并沿X轴标记抗原信息。(C) ELISA测定各肽诱导的HD和COVID-19中重度疾病患者外周血细胞IFN-γ浓度的平均值。(D)小提琴图显示了HD和COVID-19中重度疾病患者各肽的反应率,IFN-γ浓度比未刺激样品高两倍。

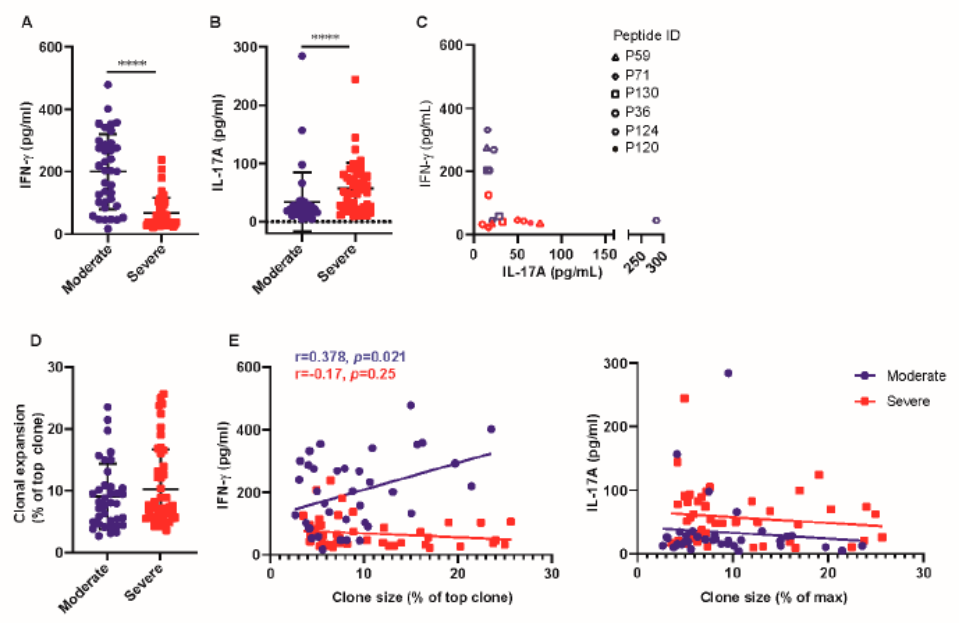
**2、严重疾病患者的T细胞反应产生更高水平的IL-17A**
(A,B)采用ELISA法检测阳性反应样品的IFN-γ (A)和IL-17A (B)水平。(C) 6个代表性样品上清液中IFN-γ与IL-17A浓度的Spearman秩相关用点阵图表示。点形状表示代表性肽,红色表示严重疾病患者,蓝色表示中度疾病患者。(D)中重度疾病患者TCR顶级克隆(免疫优势TCR β链V-J基因对)分析。(E)分析中重度疾病患者中顶端TCR克隆与IFN-γ或IL- 17A的Spearman等级相关性。
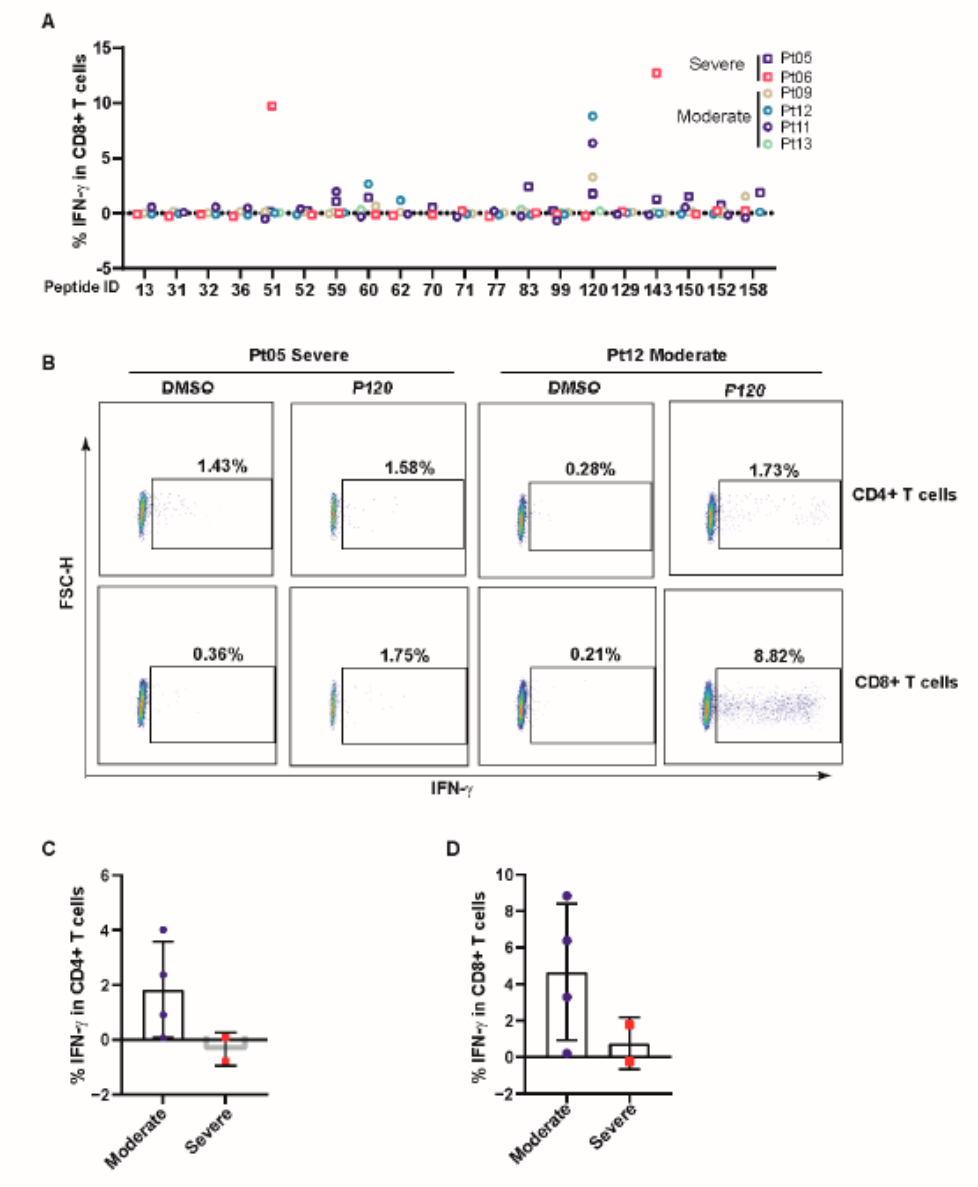
**3、COVID-19患者广泛识别保守的P120肽**
(A)用20种多肽(10 ug/mL)孵育短期细胞系5 h,流式细胞术检测IFN-γ的表达。(B) P120肽诱导的中重度疾病患者CD4+或CD8+ T细胞中IFN-γ表达的代表性流式细胞术结果。(C,D) p120特异性流式细胞术检测CD4+或CD8+ t细胞水平。通过减去阴性对照计算抗原特异性T细胞的值。
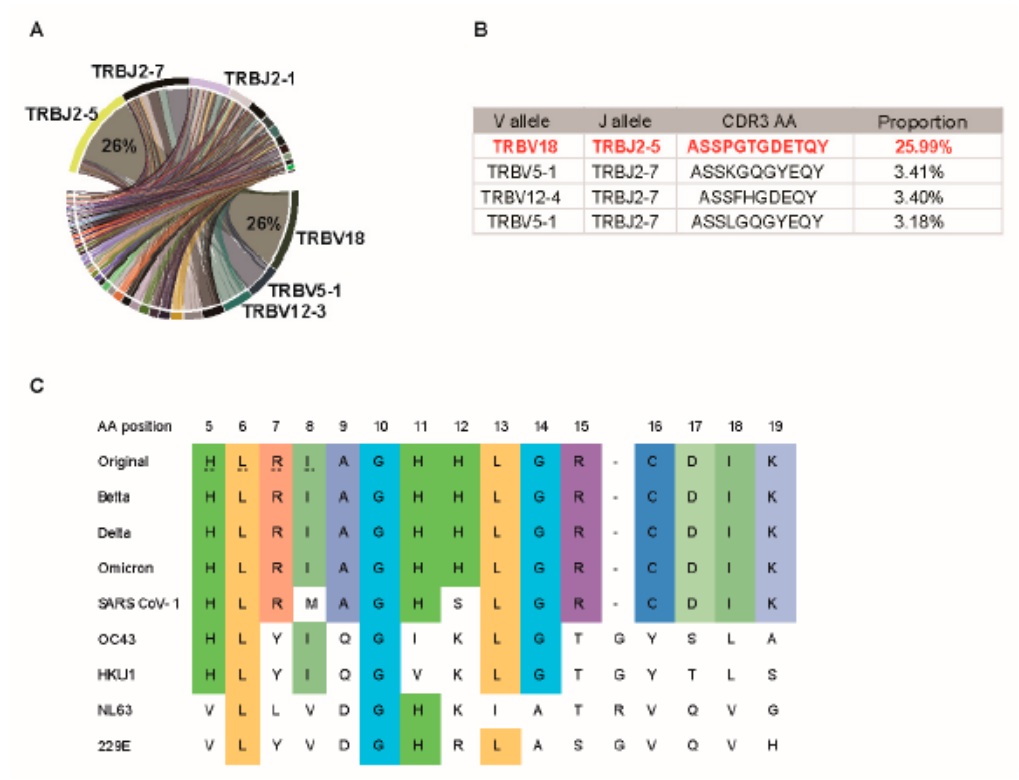
**4、P120肽在SARS-CoV-2变异体中具有保守性,可诱导强TCR扩增**
(A) Circos图描绘了P120反应样品中每个β VJ基因的使用情况。(B) P120肽短期细胞前4个CDR3序列所占比例。(C)原SARS-CoV-2 P120肽与Delta、Omicron变体、SARS-CoV-1和人类地方性冠状病毒的氨基酸序列比对。
### 讨论与展望
在本研究中,患有中度疾病的COVID-19患者比患有重度疾病的患者产生更多的IFN-γ(中度vs.重度疾病,p < 0.0001;中度vs重度,p < 0.0001),但IL-17A低于重度(p < 0.0001)。在中度COVID-19患者中,IFN-γ的产生与T细胞克隆扩增呈正相关(r = 0.3370, p = 0.0214),而在重度COVID-19患者中,IFN-γ的产生与T细胞克隆扩增无正相关(r = - 0.1700, p = 0.2480)。使用流式细胞术,研究发现M蛋白的保守肽(肽-120,P120)是CD8+ T细胞在中度疾病患者中识别的显性表位。
**结论**:协同IFN-γ的产生和SARS-CoV-2特异性T细胞的克隆扩增与COVID-19疾病的缓解有关。本研究结果有助于更好地了解COVID-19中T细胞介导的免疫,并可能为未来管理和预防SARS-CoV-2感染严重后果的策略提供信息。
*参考文献:1.https://www.mdpi.com/1999-4915/16/7/1006*


